近日,河南省神经变性病生物标志物检测与诊断重点实验室再次在国际知名期刊《Analytical Chemistry》(Anal. Chem.,影响因子 6.7,中科院 1 区)发表研究成果,成功开发一种高稳定性荧光 - 比率电化学双模式探针(Re-PS),实现阿尔茨海默病(AD)模型小鼠脑微透析液中过氧化氢(H2O2)的精准检测。该成果为阿尔茨海默病氧化应激机制研究提供了关键技术支撑,由化学化工学院董辉、张银堂、李朝辉及周艳丽团队完成,第一作者为吕晓宇,通讯作者为董辉博士。
阿尔茨海默病是最常见的神经退行性疾病,氧化应激失衡是其重要发病机制。过氧化氢作为核心活性氧(ROS)分子,在AD患者脑组织中异常累积,直接诱导神经元损伤、加速 β- 淀粉样蛋白沉积。精准检测脑内 H₂O₂水平,对 AD 早期诊断、发病机制研究及治疗效果评估至关重要。现有检测方法存在稳定性差、易受干扰、无法实时动态检测等局限。
为突破现有技术瓶颈,研究团队创新性设计 Re-PS 探针,以试卤灵(Re)为双信号报告单元,五氟苯磺酰基(PS)为H2O2特异性响应基团。PS 基团中氟原子的强吸电子效应,大幅提升探针稳定性,有效避免非特异性水解;与 H2O2发生特异性亲核取代反应后,释放 Re 并触发荧光 “开启” 与比率电化学信号变化。实验数据显示,荧光模式检测限低至 50 nM,电化学模式检测范围 1.0–50 μM,且对其他活性氧、生物分子无交叉反应。应用于AD模型小鼠脑微透析液检测,结果显示 AD 小鼠脑内H2O2水平(28.6±3.2 μM)显著高于野生型小鼠(10.3±1.8 μM)。
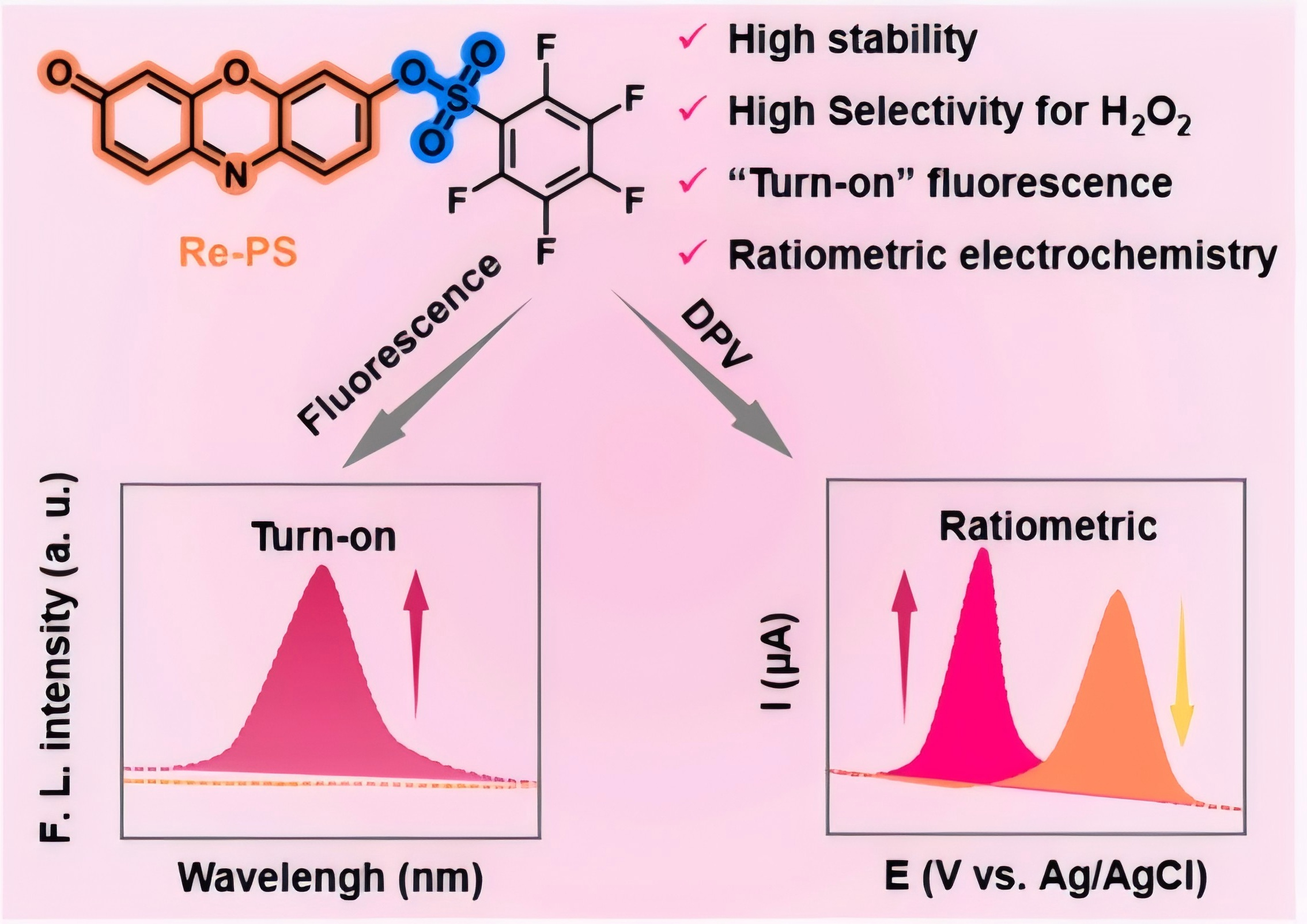
该探针的核心创新在于:一是高稳定性,磺酰酯键结构显著优于传统酯类探针,减少假阳性信号;二是高特异性,独特反应机制避免与其他活性氧交叉反应;三是双模式协同,荧光实时成像结合比率电化学精准定量,适配体内外多场景检测。此项研究为解析 AD 氧化应激机制提供了直接检测工具,也为神经退行性疾病相关活性氧检测提供了通用策略。
该工作得到国家自然科学基金、河南省自然科学基金、河南省高校科技创新人才等项目资助。
(供稿:董辉 一审:刘孜 二审:朱旭 三审:周艳丽)
